您现在的位置: 百济新特药房网首页 >> 行业资讯 >> 新药快讯
一线治疗鼻咽癌!恒瑞医药PD-1单抗即将获批
- 来源: 百济药房药讯 作者:百济动态 浏览: 发布时间:2020/11/9 14:14:00
2020年11月6日,国家药监局药品审评中心(CDE)网站公示信息显示,恒瑞医药的注射用卡瑞利珠单抗拟纳入优先审评审批程序。
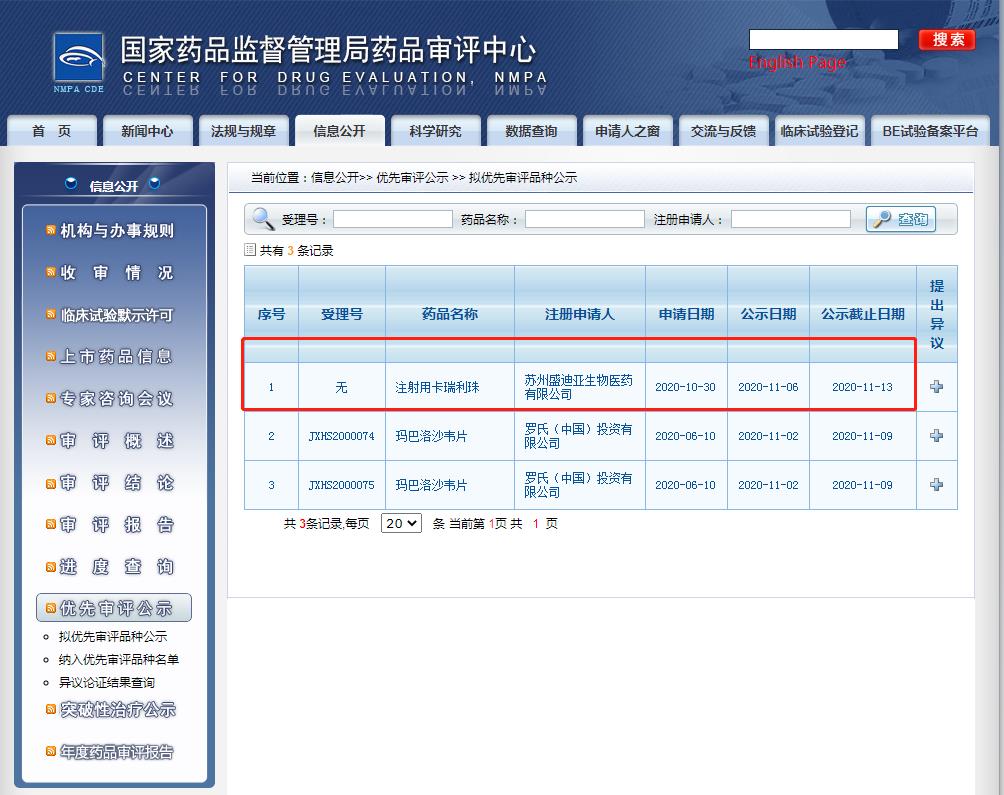

截图来源:CDE官网
拟优先审评的理由是:同意按优先审评范围“(六)国家药品监督管理局规定其他优先审评审批的情形”纳入优先审评审批程序。
值得一提的是,在今年的9月份,卡瑞利珠单抗“用于既往接受过二线及以上化疗后疾病进展或不可耐受的晚期鼻咽癌患者的治疗”申请,已因“符合附条件批准的药品”被CDE纳入优先审评。
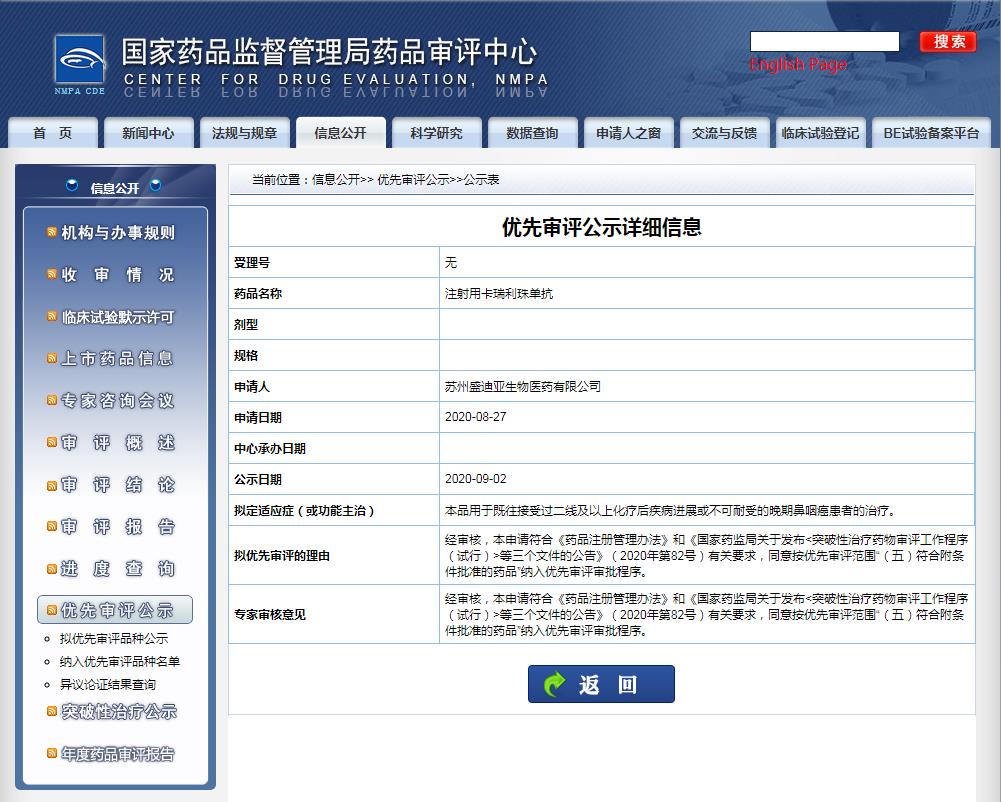
截图来源:CDE官网
卡瑞利珠单抗是恒瑞医药是恒瑞医药旗下的重点研发产品,自2019年5月首次在中国获批上市以来,目前已在中国获批四个适应症,分别为:
1)用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者的治疗;
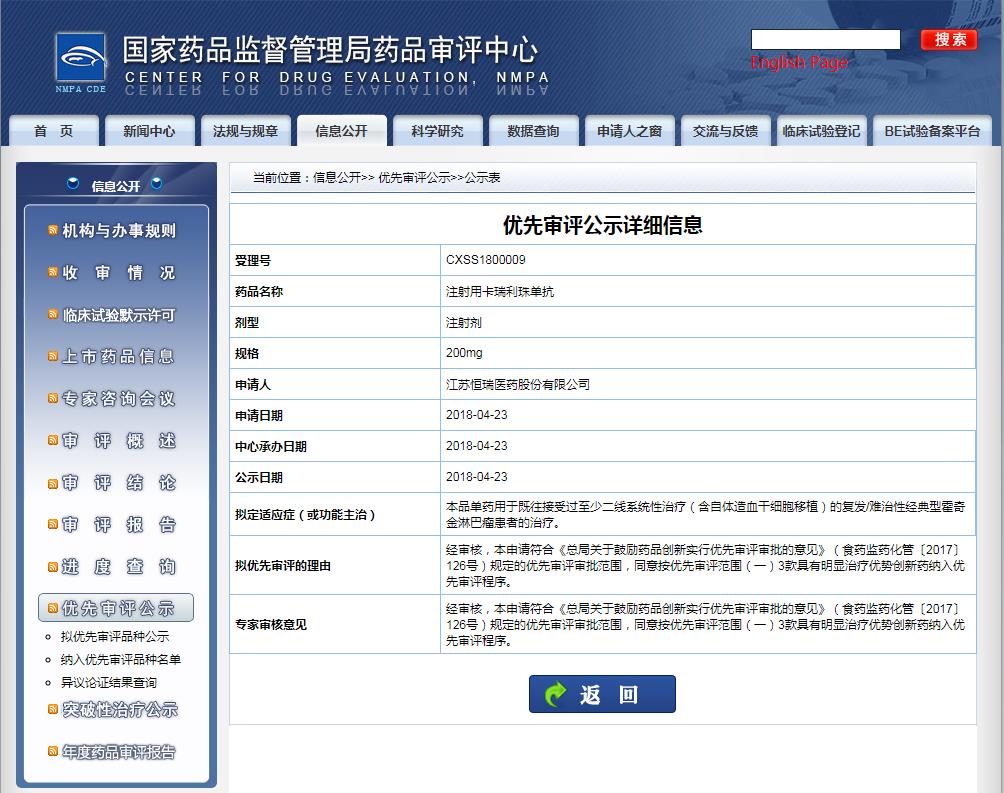
截图来源:CDE官网
2)用于既往接受过标准系统性治疗后疾病进展或不可耐受的晚期肝细胞癌患者的治疗;

截图来源:CDE官网
3)联合培美曲塞和卡铂用于EGFR基因突变阴性和ALK阴性的、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌的一线治疗;
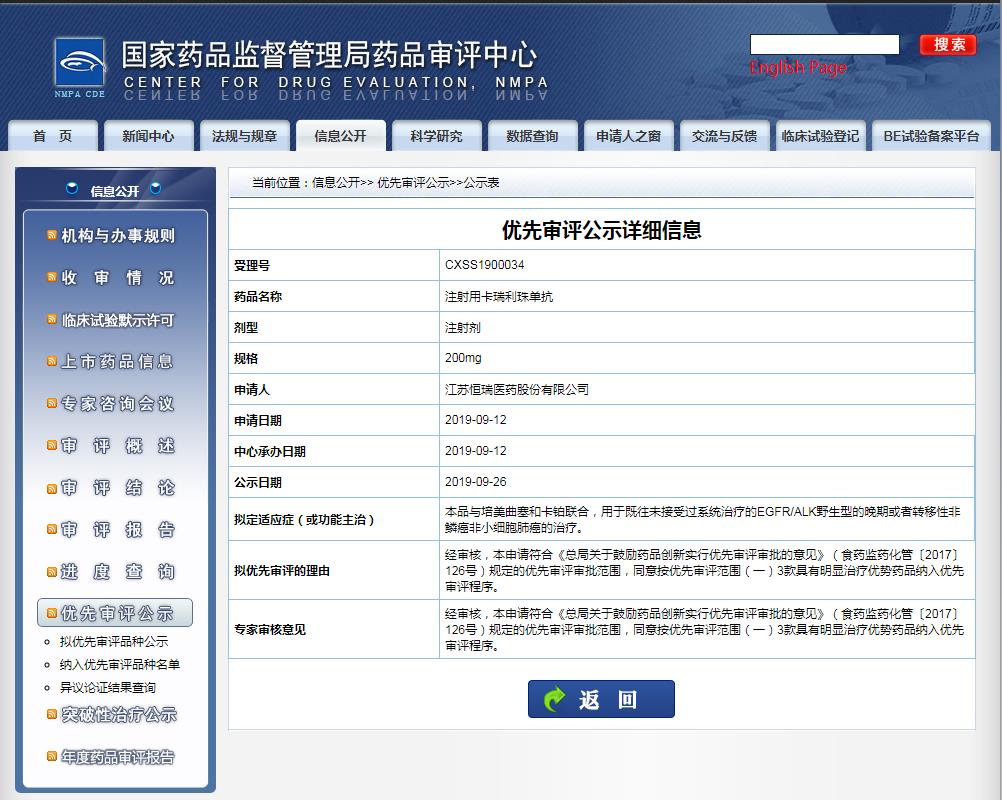
截图来源:CDE官网
4)用于既往接受过一线标准化疗后疾病进展或不可耐受的局部晚期或转移性食管鳞癌患者的治疗。
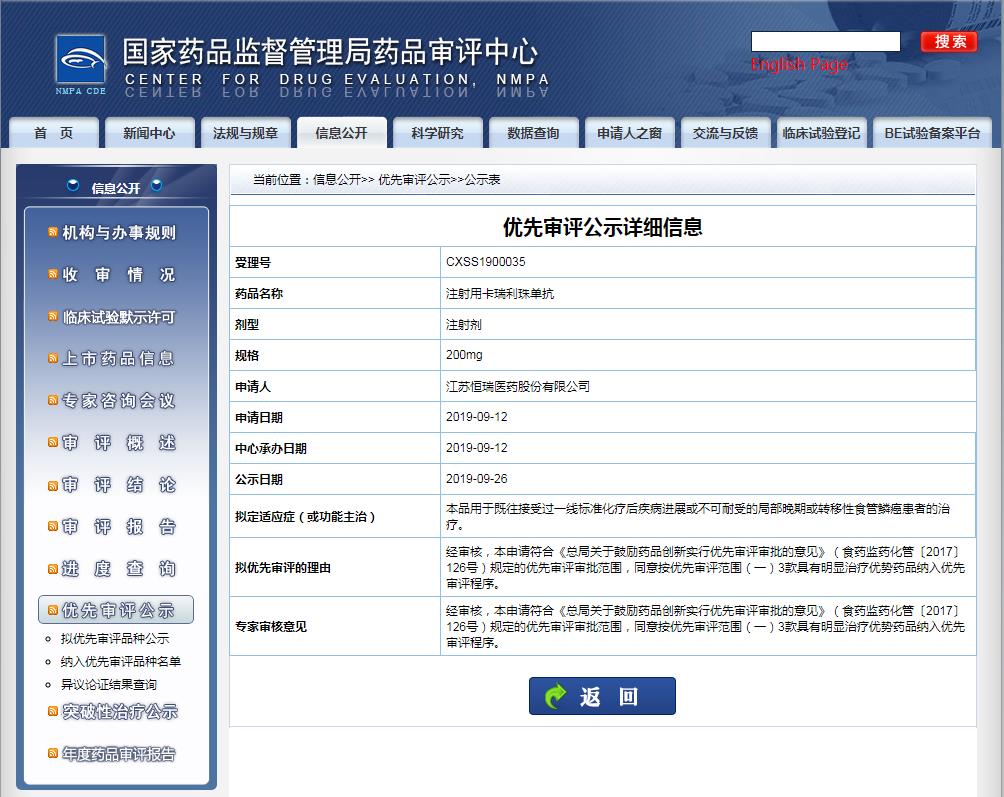
截图来源:CDE官网
卡瑞利珠单抗针对不同鼻咽癌适应症是申请被纳入优先审评以及拟优先审评意味着,该药有望惠及更多的癌症患者。
鼻咽癌是中国高发肿瘤之一。放射治疗是治疗早期鼻咽癌的主要方法,但大约20%-37%的患者会出现局部复发或者远处转移。复发或转移鼻咽癌的治疗手段非常有限,预后较差,目前一线标准治疗一般是含铂双药化疗,患者无进展生存期为7个月左右。中国鼻咽癌患者亟需更多的治疗手段延长生存期。
祝贺恒瑞医药卡瑞利珠单抗一线治疗晚期鼻咽癌的新适应症申请拟被纳入优先审评,希望该药早日获批,给中国鼻咽癌患者带来新的希望。








