您现在的位置: 百济新特药房网首页 >> 行业资讯 >> 百济新闻
落实“两票制”:超90%药批、CSO将消失!
- 来源: 百济药房药讯 作者:百济动态 浏览: 发布时间:2018/10/18 10:38:00
关于“两票制”的最 新 部署来了。
据健康报报道,10月15日,2018年全国药政工作会议召开,国家卫生健康委员会副主任曾益新指出,按照政府部署,下半年药政工作将从使用端发力,把药品供应保障制度建起来、把不合理用药费用降下来。

会议明确近期我国药政工作将着力围绕七方面展开,特别强调各地卫生健康行政部门要全面落实药品采购“两票制”,配合有关部门加强信息互联互通、打击过票洗钱等违法行为。
这既是对年初机构改革以来,医保局组建、医改办重组后,业界对“两票制”去留疑问的回应,也明确了国家层面对打击挂靠、走票等药品流通领域违法行为的态度。而这也被认为是解决药价虚高关键。
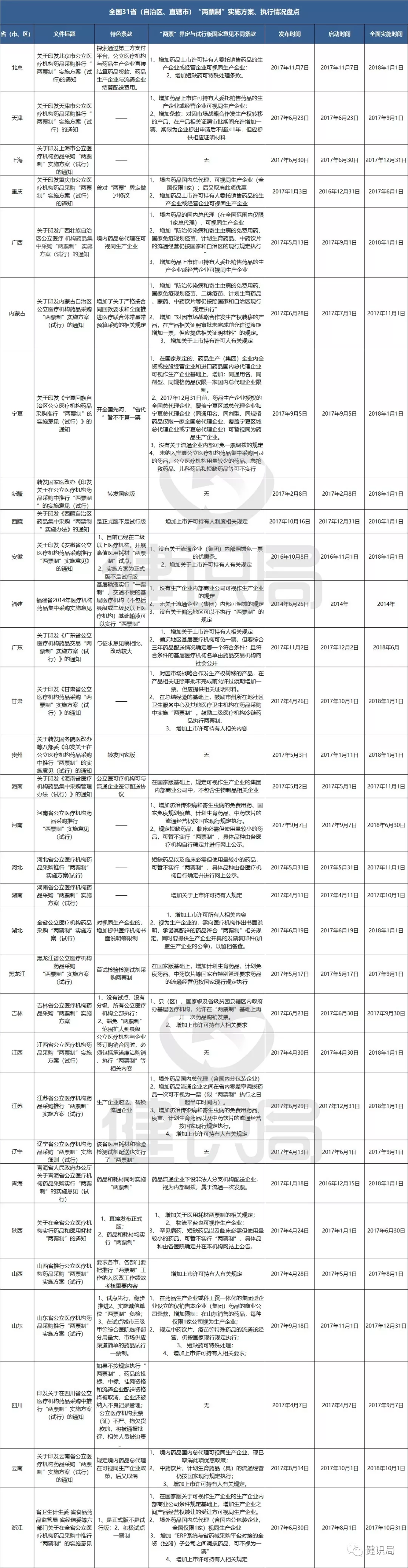
“两票制”是剑指药品流通领域“挂靠、走票”顽疾的政策,虽然2017年1月9日正式全国推行后,曾一度遭到业界反对,但并未影响进程,历时10个月,截至2017年11月7日,全国31个省、直辖市、自治区均已明确实行药品“两票制”,并列出时间表,陕西等省份还开始了医用耗材“两票制”试点。
到了今年年初,由于“两票制”的牵头单位——医改办、国家卫计委等部门都涉及机构改革,业界一度认为,随着医药服务和价格社会治理格局的形成,大市场监管环境的确立,“两票制”这一行政权利,作为阶段性政策,对药品流通行业的洗牌、购销秩序重塑、清理“走票、挂票”乱象的作用,或可由市场化的手段替代,其推进或遭搁置。
根据各省市陆续公示的“两票制”实施时刻表,截至2018年10月1日,我国31省、直辖市、自治区应已全部进入“两票制”实施阶段。分析人士指出,无论各地进度此前是否有所迟滞,未来都将进入全速前进阶段,而大批心怀侥幸,仍靠虚开发票、洗钱生的假CSO等,将迎来寒冬。

昨天召开的2018年全国药政工作会议明确,近期我国药政工作将着力围绕7个方面重点展开。除了全面落实药品“两票制”,短缺药预警、推动基药制度落地、保障抗癌药供应等都是重点。
● 要加快监测预警网络体系建设,启动医疗机构短缺药品信息直报,完善四级监测预警机制;开展新一轮短缺药品基础信息核查,将临床必需、短缺影响大的药品纳入重点监控目录。完善短缺药品应对机制,推动落实短缺药品直接挂网采购制度,建立失信经营者黑名单制度、短缺药品清单管理制度,各地要组织落实短缺药品供应保障工作督查考核和激励问责。
● 各地要尽快研究制定具体措施,将国家基本药物制度实施情况纳入政府绩效考核体系,围绕新版国家基本药物目录制定基本药物配备使用、招标采购、监测评价、考核评估等配套文件并组织实,全面推进基本药物制度落地。国家将组织开展以市或县为单位的基本药物制度综合试点;修订编制2018年版基本药物临床应用指南和处方集并组织培训。各省级卫生健康行政部门要合理确定各级各类医疗机构国家基本药物的使用比例。
● 遴选成立国家药品临床综合评价专家委员会,依托国家药物和卫生技术综合评估中心、国家临床重点专科医疗机构等单位,确立评价体系总体架构,以基本药物为重点,编制评价工作方案。
● 各地卫生健康行政部门要全面落实药品采购“两票制”,督促医疗机构在药品验收入库时做好“两票”的留存备查工作,配合有关部门加强信息互联互通、打击过票洗钱等违法行为。
● 增强医疗机构药学服务能力,推动医疗机构总药师试点,加强药学人员继续教育,推动药事服务收费项目设置。
● 推进国家药物政策体系和协调机制建设,在基本药物、短缺药品、仿制药和儿童用药、罕见病用药等供应保障及使用政策方面,发挥好协调牵头作用。

随着“两票制”、“金税三期”、“营改增”的落地,各地药批、CSO正在逐渐消失。
据健识君的不完全统计,全国目前还有1.19万家商业公司,仅2017年就消失了1050多家。
与行业早已存在的部分靠过票、洗钱为生的药批不同, CSO(合同营销组织),本来是为医药企业提供市场调研,策略分析、制定等服务的合规组织。但在“两票制”改变药品领域格局后,这一行业变了味儿。很多扎堆组建的CSO以医药类资讯公司之名,为药企提供“过票、洗钱”服务。目前此类CSO已成为有关部门打击重点。
医药CSO联盟数据显示,截至8月,全国14万家的医药CSO企业仅10万家存续,有25.4%的CSO半路“失踪”。其中,7651家被吊销营销营执照,10709家被注销营销执照,6840家被记为经营异常,1272家有官方行政处罚记录。泰凌、康哲等起家较早、规模较大的CSO公司,在经历巨额处罚、业绩滑坡之后,也已谋求转型。
业界认为,“两票制”是对医药行业影响的政策,而随着国家卫健委明确此项工作仍为近期药政工作重点,行业洗牌也将持续推进。根据原CFDA监管司司长李国庆此前所说,我国1.3万家批发企业中,预计至少退出1万家将遭淘汰。而CSO的淘汰率或将更高。
来源:健识局 原创:木木
本文为转载,我们不对其内容和观点负责。








