您现在的位置: 百济新特药房网首页 >> 糖尿病 >> Ⅱ型糖尿病 >> Ⅱ型糖尿病治疗与研究进展
沙格列汀的临床研究进展
- 来源: 百济药房药讯 作者:百济动态 浏览: 发布时间:2014-5-26 14:26:00
陆菊明
2008年中华医学会糖尿病学分会(CDS)组织的糖尿病流行病学调查结果显示,在20岁以上的人群中,年龄标化的糖尿病患病率为9.7%,而糖尿病前期的比例更高达15.5%,相当于每4个成年人中就有1个高血糖状态者,但仅有1/4的糖尿病患者HbA1c达标(<6.5%)
T2DM发病和进展的一个重要原因是胰岛功能进行性衰退,包括β细胞胰岛素分泌缺陷和α细胞胰高血糖素分泌增加造成的胰岛素与胰高血糖素比例失调。
对于许多T2DM患者,单药口服治疗不能维持血糖控制目标。UKPDS指出,尽管T2DM患者控制饮食,服用磺脲类药物、二甲双胍等进行治疗,仍不能阻止β细胞功能恶化的进程,血糖逐渐失去控制,进而需要联合降糖效果更显著的药物治疗并最终使用胰岛素。因此,需要探索更新、更有效的治疗手段。
一、肠促胰素系统
由胃肠道细胞分泌的肠促胰素包括GLP-1和葡萄糖依赖性促胰岛素释放多肽(GIP)是两种重要的肠促胰素,在食物中营养物质的刺激下分泌释放入血液,通过葡萄糖依赖性方式促胰岛素分泌来调节血糖稳态。GLP-1具有葡萄糖依赖性促胰岛素分泌的特性,其促胰岛素分泌作用在血糖浓度升高时出现,血糖浓度恢复正常则消失;同时,GLP-1还可促进β细胞增殖,抑制其凋亡,增加胰岛素合成、改善β细胞功能。然而,体内产生的活性GLP-1半衰期仅为1.5~2min,其氨基末端前两个氨基酸可被二肽基肽酶(DPP-4)快速裂解而失去促胰岛素分泌活性,使得内源性活性GLP-1无法在体内达到治疗浓度;因此抑制DPP-4从而延长内源性GLP-1和GIP持续作用时间作为药物开发的新靶点被人们所重视。由此,一种新型机制的降糖药物---DPP-4抑制剂应运而生。
沙格列汀(saxagliptin,sax)是一种强效、选择性DPP-4抑制剂,可特异性延长对DPP-4的抑制,从而延长内源性GLP-1和GIP持续作用时间,降低血糖。2011年5月5日,Sax在中国获得上市批准(商品名:安立泽),用于治疗T2DM。GLP-1、GIP、GLP-1类似物比较见表1。
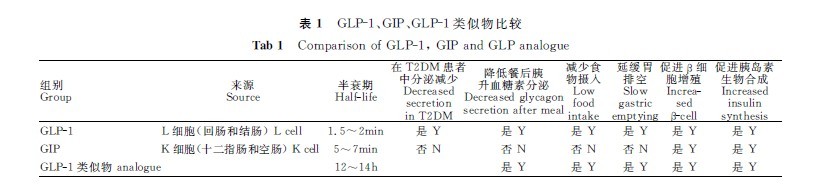
二、Sax的药代动力学Sax的血浆浓度具有剂量依赖性,且对于健康受试者和T2DM患者,其药代动力学参数相似。在T2DM患者中,Sax抑制DPP-4活性长达24h。在口服葡萄糖或进餐后,Sax对DPP-4的抑制作用导致GLP-1和GIP的活性水平增加2~3倍,并且能降低胰升血糖素浓度,葡萄糖依赖性地增加胰腺β细胞分泌胰岛素。达到最大血浆药物浓度的时间为<2h,且计算的平均半衰期为2.2~3.8h。进一步研究证明老年受试者(≥65岁)与年轻受试者(18~40岁)相比,在接受单剂量为10mg的治疗后其暴露量的升高不到2倍,因此不需要根据年龄调整剂量。
约70%的Sax可在尿液中回收,表明口服给药可被广泛吸收。近期有一项研究评价了肾功能不全和血液透析对Sax药代动力学的影响;对于轻度肾功能不全受试者,Sax及其主要代谢产物的整体系统暴露量(AUC)均值分别是正常肾功能受试者体内AUC均值的1.2倍和1.7倍;对于中度肾功能不全受试者,AUC值分别是正常肾功能受试者的1.4倍和2.9倍;在重度肾功能不全受试者体内的相应值分别达2.1倍和4.5倍。4h的血液透析可去除23%剂量的Sax。
三、Sax临床研究为对Sax的降糖疗效进行了评价,进行了包括4000多名T2DM 患者的Ⅱ/Ⅲ期全面的临床试验研究。
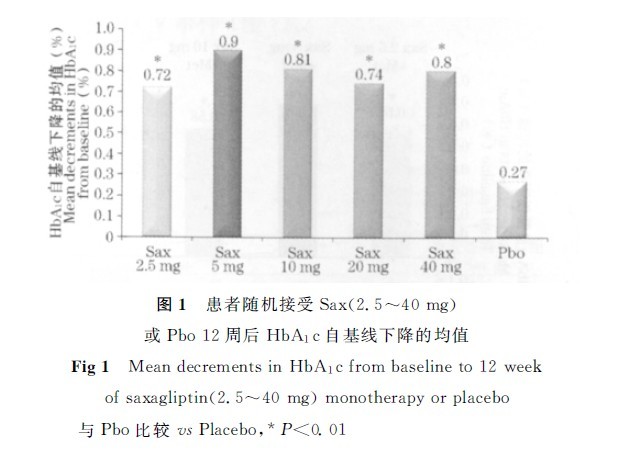
1。单药治疗:患者随机分组使用Sax(2.5~40mg/d)或安慰剂(Pbo)治疗12周,Sax2.5mg、5mg、10mg、20mg、40mgg组HbA1c较基线分别平均下降0.72%、0.90%、0.81%、0.74%、0.80%(p<0.01),Pbo组HbA1C下降的均值为0.27%(图1)。
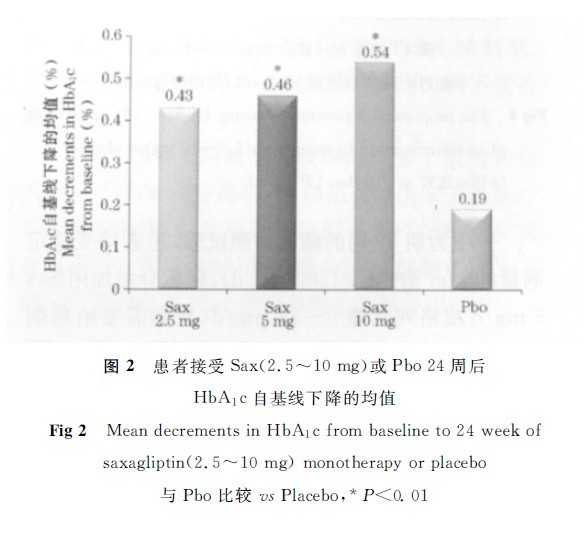
一项24周的III期研究中,未经治疗的患者接受Sax单药2.5mg、5mg、10mg治疗各组的HbA1C较基线分别平均下降0.43%、0.46%、0.54%,Pbo组HbA1C下降的均值为0.19%与Pbo组相比,Sax各剂量组HbA1C水平均明显降低(p<0.01);35% ~41% 患者的HbA1C达到<7.0%,Pbo组为24%(图2)。
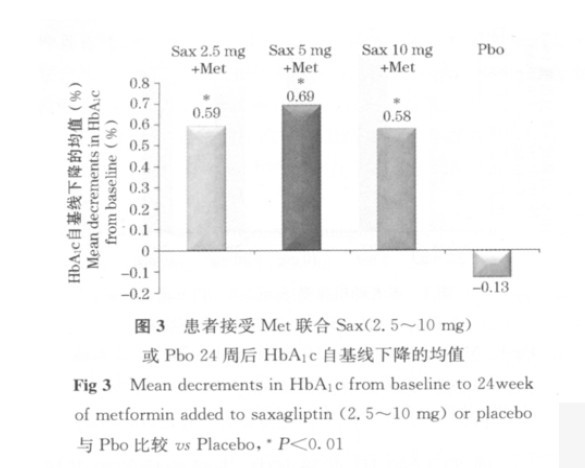
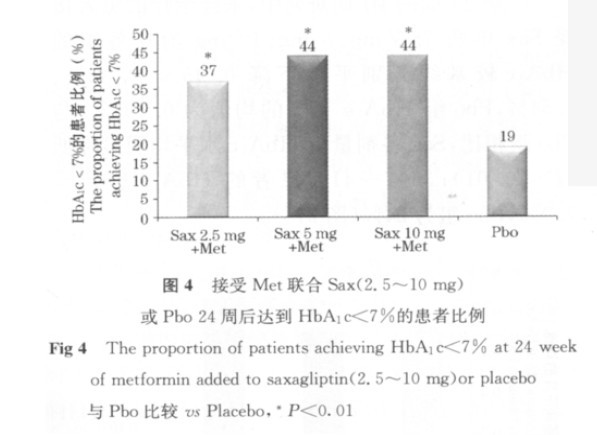
2.联合治疗:一项24周的Ⅲ期双盲、Pbo对照研究中,对单用二甲双胍(Met)血糖控制不佳的T2DM 患者,加用Sax2.5mg、5mg、10mg各组的HbA1C较基线平均下降0.59%、0.69%、0.58%,而Pbo组上升0.13%,疗效显著优于Pbo组(p<0.01)(图3)。Sax各组分别有37%和44%的患者HbA1C<7.0%,高于Pbo组(p<0.01)(图4)。
一项为期52周的随机对照试验,患者接受稳定剂量的Met治疗(≥1500mg/d),随机分组加用Sax5mg/d或格列吡嗪5~20mg/d(根据需要给药剂量逐步增加)。结果与基线水平相比,Sax组与格列吡嗪组校正的HbA1c化均值分别为-0.74%和-0.80%,疗效相当。
一项涉及768例患者的Ⅲ期临床试验,患者接受7.5mg/d开放标签的格列本脲,随机加用剂量为2.5mg或5mg/d的Sax组和增加格列本脲的剂量为10mg/d组。结果显示,联合用药组比格列本脲增量组降低HbA1c更有效。另外,格列本脲剂量递增组中30%的患者由于未能达到血糖控制目标而退出研究,联合用药组中,18%和17%的患者由于上述原因而退出研究。
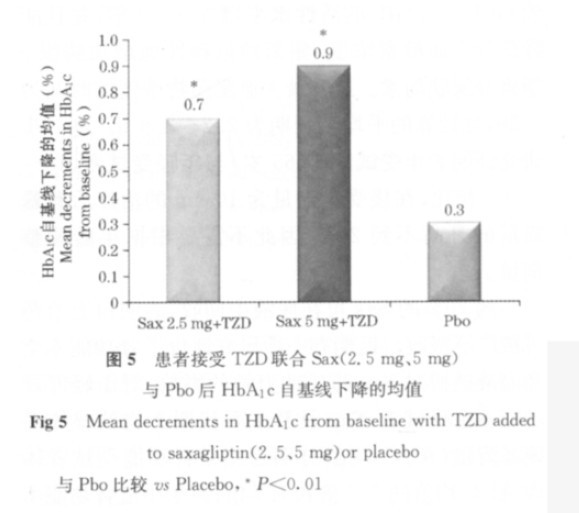
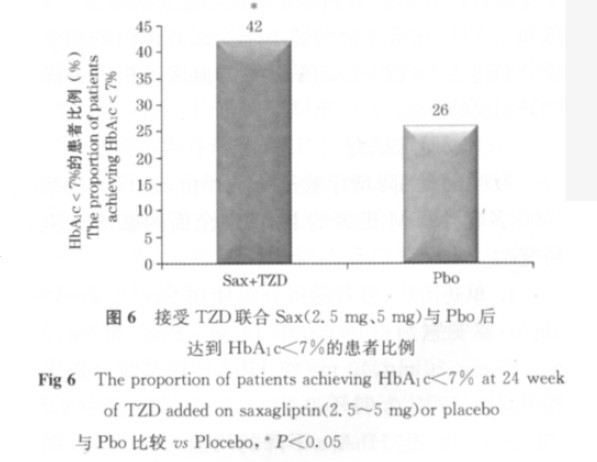
在另一项Ⅲ期试验中,565例接受稳定剂量的TZD(吡格列酮或罗格列酮)单药治疗,HbA1c基线在7.0%~10.1%。与Pbo相比,加用剂量为2.5或5mg/d的Sax组HbA1c自基线分别下降0.7%和0.9%(与Pbo相比p<0.01),Pbo组下降的均值为0.3%(图5)。Sax组达到HbA1c<7.0%的患者为42%,Pbo组为26%(组间比较,p<0.05)(图6)。
四、不良反应Sax耐受性良好,对血脂、血压、心率均无影响,无肝脏、胰腺、骨骼肌和肾脏的安全性问题。在一项I期研究中,给予T2DM患者2周50mg(推荐治疗剂量的10倍)的治疗,未发现与剂量相关的不良事件或实验室异常(包括对校正的QT间期的影响作用)。在III期试验中报告最多的不良事件为头痛。
Sax无论作为联合治疗或单药治疗时,不良事件特征均相似,尤其是在联合应用中,Sax和Pbo的不良事件发生率相近。
1.低血糖:在Ⅲ期随机对照试验中,与二甲双胍联合治疗时,Sax(2.5~10mg/d)组有0.5%的患者、Pbo组有0.6%的患者出现确认的低血糖(血糖浓度≤ 2.8mmol/L)。Sax联合Met治疗的患者,52周内只有3.0%的患者出现过一次以上低血糖,而对照组(格列吡嗪与Met联合)的为36.3%,两组差异具有统计学意义(P<0.01)。对于应用稳定剂量的TZD进行治疗的患者,加用剂量为2.5或5mg/d的Sax时,分别有4.1%和2.7%的患者发生低血糖事件,Pbo组为3.8%.单药治疗(2.5~40mg/d)没有确认的低血糖病例,且各剂量出现低血糖事件的比例与Pbo相似。
2。心血管事件:UKPDS、控制糖尿病心血管危险行动(ACCORD)、糖尿病与心血管疾病行动(ADVANCE)以及退伍军人糖尿病试验(VADT)等大型研究均未能证明强化降糖治疗对大血管事件有益。美国食品药品监督管理局(FDA)2008年12月就制药公司如何使用临床试验来证明其研发的T2DM 新药,在治疗过程中不会带来增加心血管方面疾病的风险公布了正式的指导原则,要求药物在申请上市前,应比较试验药物和对照组的重要心血管事件发生率,评估预计风险比的双侧95%可信区间(95%CI)。
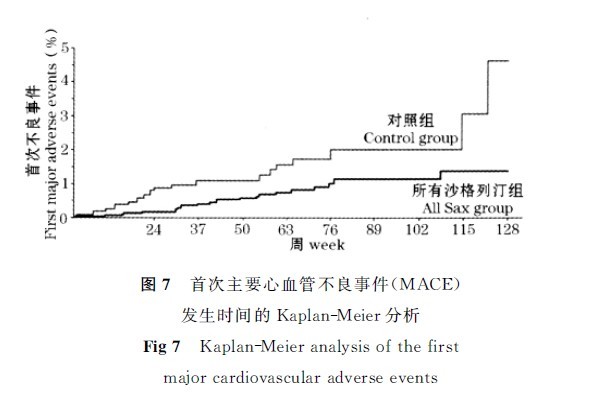
Sax的一项回顾性分析纳入8项Ⅱ/Ⅲ期的临床试验,包括1项为期12周、给药剂量范围为2.5~100mg/d的Ⅱ期试验,6项相似设计的Ⅲ期试验(2项单药治疗试验,在Met、格列本脲和TZD的基础上联合治疗各1项研究以及1项与Met起始联合用药的研究)及1项作用机制(高血糖钳夹试验)研究。共计包括4例患者,随机分为Sax(2.5~100mg/d)组3356例,对照组1251例(Pbo656例,Met组328例,剂量递增的格列本脲组267例),结果有61例患者(Sax组38例,对照组23例)出现心血管事件;41例患者(Sax组23例,对照组18例)出现心血管(CV)死亡/心肌梗死(MI)/卒中事件[95%CI为0.44(0.24~0.82)]。Sax组和对照组CV死亡、MI和卒中的组成比例分别是:7例(0.2%)vs 10例(0.8%),8例(0.2%)vs 8例(0.6%)和11例(0.3%)vs 5例(0.4%)。在广泛开展的药物研发计划中,随机分配入Sax组的患者CV死亡/MI/卒中风险未增加。尽管本项系统回顾分析具局限性,但得出的数据支持应用Sax治疗可潜在的减少CV事件(图7)。
3。对体重的影响:在与Met联合治疗的Ⅲ期研究中,剂量为2.5、5和10mg/d的Sax治疗至第第24周体重分别下降均值1.43、0.87和0.53kg,平均1.1kg,与格列吡嗪联合Met治疗的患者体重平均上升1.1kg比,差异具有统计学意义(P<0.01);Pbo组为0.92kg。
五、Sax的推荐剂量Sax是首个被我国SFDA 批准具有单药和与Met联合治疗T2DM 双适应证的DPP-4抑制剂。
推荐剂量为5mg,每日一次给药。服用时间不受进餐影响。
目前,DPP-4抑制剂已被国内外多个机构和组织纳入T2DM治疗路径,特别是英国国家卫生医疗质量标准署建议,在患者无法耐受多项治疗或存在显著的低血糖风险时,可考虑DPP-4抑制剂作为一线治疗药物以及Met治疗基础上的联合用药。
参考文献:陆菊明.沙格列汀的临床研究进展[J].中国糖尿病杂志,2012,4,20(4):316-319
TAG:安立泽 沙格列汀 沙格列汀的临床研究进展
相关药品

便民帮助- 常见问题 | 服务指南 | 药学服务 | 顾客意见 | 顾客投诉 | 专科服务 | 寻医问药 | 药师窗口
专科分类服务- 肿瘤科 | 肝病科 | 神经科 | 精神科 | 皮肤性病科 | 眼 科 | 风湿免疫科 | 心血管科 | 糖尿病科 | 其他科用药
药品导购服务- 肿瘤科药品 | 精神科药品 | 肝病科药品 | 眼科药品 |皮肤性病科药品 | 神经科药品 | 风湿免疫科药品
药房资质- 企业法人营业执照 | 药品经营许可证 | 药品经营质量管理规范认证 | 食品卫生许可证 | 互联网药品信息服务资格证







